Pernah nggak sih, lihat iklan makanan yang bikin air liur langsung menetes? Atau penasaran kenapa plastik bisa lentur dan dibentuk jadi berbagai macam barang? Nah, semua itu ada hubungannya sama reaksi adisi, lho!
Reaksi ini emang nggak sesederhana kelihatannya. Ada mekanisme rumit di baliknya, contohnya beragam, dan aplikasinya pun luas banget. Tapi tenang, di artikel ini kita bakal kupas tuntas semuanya! Dijamin, setelah baca ini, kamu bakal paham betul apa itu reaksi adisi, mekanismenya gimana, contoh-contohnya apa aja, dan kenapa reaksi ini penting banget dalam dunia kimia dan industri. Yuk, simak!
Apa Itu Reaksi Adisi?
Sederhananya, reaksi adisi adalah reaksi penggabungan dua molekul atau lebih menjadi satu molekul yang lebih besar. Kata kuncinya di sini adalah "penggabungan". Molekul-molekul kecil "menempel" pada molekul yang lebih besar tanpa ada atom yang hilang.
Biasanya, reaksi ini terjadi pada senyawa yang memiliki ikatan rangkap (ikatan ganda atau ikatan tiga), seperti alkena dan alkuna. Ikatan rangkap ini "dibuka" dan atom-atom dari molekul lain ditambahkan ke atom karbon yang tadinya berikatan rangkap.
Mekanisme Reaksi Adisi
Mekanisme reaksi adisi bisa berbeda-beda tergantung pada jenis reaktan dan kondisi reaksi. Tapi, secara umum, ada dua mekanisme utama:
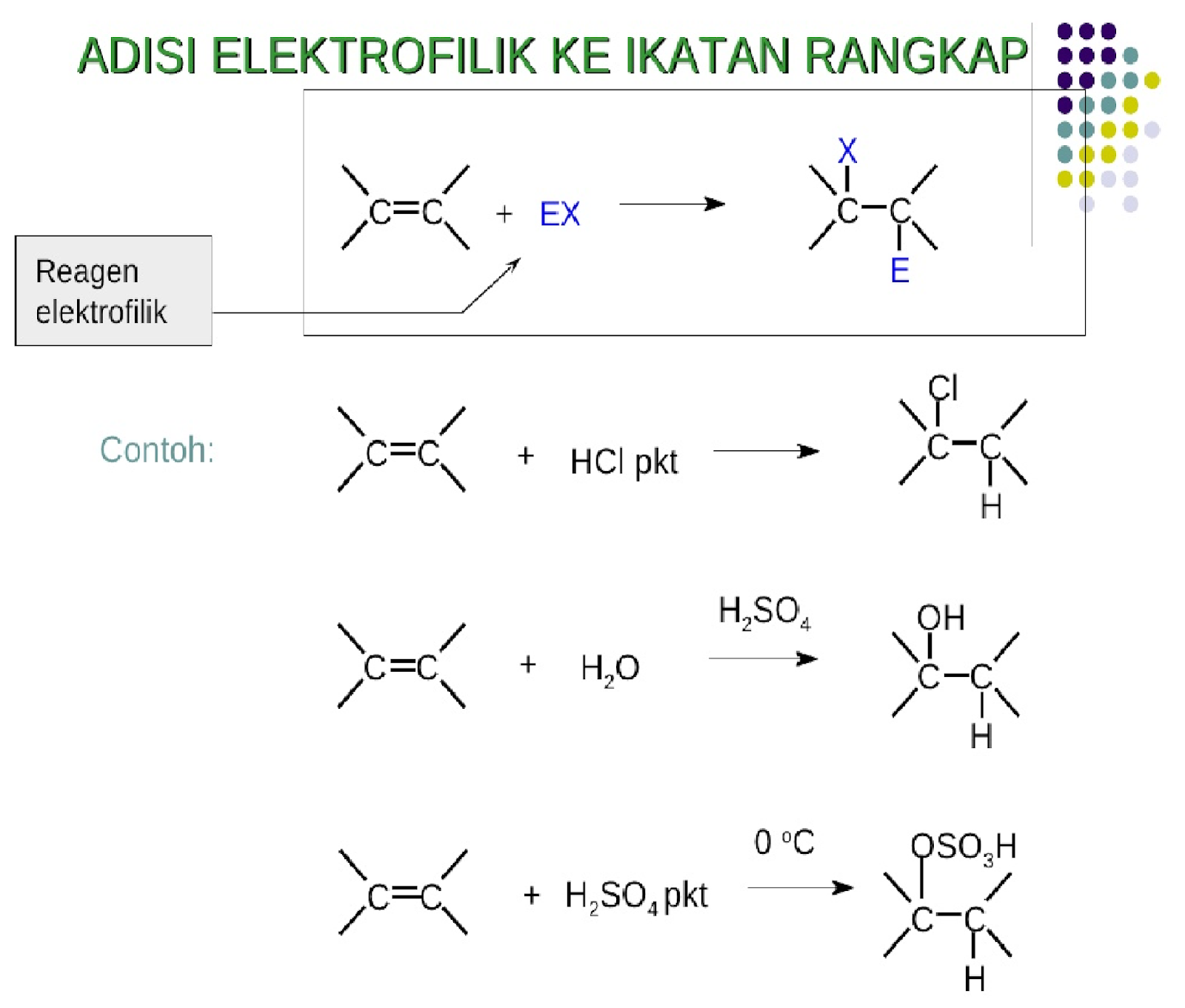
Adisi Elektrofilik
Adisi elektrofilik adalah mekanisme yang paling umum terjadi pada alkena dan alkuna. Dalam mekanisme ini, elektrofil (spesies yang kekurangan elektron) menyerang ikatan rangkap yang kaya elektron.
-
Tahap 1: Serangan Elektrofil. Elektrofil, yang biasanya berupa ion positif atau molekul polar, mendekati ikatan rangkap. Kerapatan elektron yang tinggi pada ikatan rangkap menarik elektrofil, menyebabkan ikatan rangkap pecah dan elektrofil terikat pada salah satu atom karbon.
-
Tahap 2: Pembentukan Karbokation. Pembentukan karbokation (ion karbon positif) terjadi pada atom karbon yang lain. Karbokation ini sangat reaktif dan rentan terhadap serangan oleh nukleofil (spesies yang kaya elektron).
-
Tahap 3: Serangan Nukleofil. Nukleofil menyerang karbokation, membentuk ikatan baru dan menyelesaikan reaksi adisi.
Contoh reaksi adisi elektrofilik adalah adisi hidrogen halida (seperti HCl atau HBr) pada alkena.
Adisi Radikal Bebas
Adisi radikal bebas melibatkan radikal bebas sebagai perantara reaksi. Radikal bebas adalah atom atau molekul yang memiliki elektron tidak berpasangan, sehingga sangat reaktif.
-
Tahap 1: Inisiasi. Radikal bebas dihasilkan melalui pemutusan homolitik (pemutusan ikatan yang menghasilkan dua radikal bebas) dari suatu molekul. Pemutusan ini biasanya diinduksi oleh panas, cahaya, atau peroksida.
-
Tahap 2: Propagasi. Radikal bebas menyerang ikatan rangkap, membentuk radikal bebas baru. Radikal bebas baru ini kemudian menyerang molekul lain, menghasilkan radikal bebas baru yang lain, dan seterusnya. Proses ini berlanjut secara berantai.
-
Tahap 3: Terminasi. Rantai reaksi dihentikan ketika dua radikal bebas bergabung, membentuk molekul stabil.
Contoh reaksi adisi radikal bebas adalah polimerisasi alkena, di mana banyak molekul alkena bergabung untuk membentuk polimer panjang.
Contoh-Contoh Reaksi Adisi
Reaksi adisi sangat beragam dan banyak ditemukan dalam berbagai bidang kimia dan industri. Berikut adalah beberapa contohnya:
Hidrogenasi
Hidrogenasi adalah reaksi adisi hidrogen (H2) pada ikatan rangkap. Reaksi ini biasanya memerlukan katalis logam, seperti nikel (Ni), paladium (Pd), atau platina (Pt). Hidrogenasi digunakan secara luas dalam industri makanan untuk mengubah minyak nabati cair menjadi lemak padat (margarin).
- Contoh: Etena (CH2=CH2) + H2 → Etana (CH3-CH3)
Halogenasi
Halogenasi adalah reaksi adisi halogen (seperti klorin (Cl2) atau bromin (Br2)) pada ikatan rangkap. Reaksi ini digunakan untuk membuat senyawa haloalkana, yang banyak digunakan sebagai pelarut dan bahan baku dalam sintesis organik.
- Contoh: Etena (CH2=CH2) + Br2 → 1,2-dibromoetana (BrCH2-CH2Br)
Hidrohalogenasi
Hidrohalogenasi adalah reaksi adisi hidrogen halida (seperti HCl atau HBr) pada ikatan rangkap. Reaksi ini mengikuti aturan Markovnikov, yang menyatakan bahwa atom hidrogen akan terikat pada atom karbon yang memiliki jumlah atom hidrogen lebih banyak.
- Contoh: Propena (CH3CH=CH2) + HCl → 2-kloropropana (CH3CHClCH3)
Hidrasi
Hidrasi adalah reaksi adisi air (H2O) pada ikatan rangkap. Reaksi ini biasanya memerlukan katalis asam, seperti asam sulfat (H2SO4). Hidrasi digunakan untuk membuat alkohol.
- Contoh: Etena (CH2=CH2) + H2O → Etanol (CH3CH2OH)
Polimerisasi Adisi
Polimerisasi adisi adalah proses penggabungan banyak molekul kecil (monomer) menjadi molekul besar (polimer) melalui reaksi adisi. Contohnya adalah polimerisasi etena menjadi polietilena (plastik).
- Contoh: n CH2=CH2 → -(CH2-CH2)n-
Aplikasi Reaksi Adisi
Reaksi adisi memiliki aplikasi yang sangat luas dalam berbagai bidang, di antaranya:
-
Industri Petrokimia: Reaksi adisi digunakan untuk menghasilkan berbagai macam bahan kimia penting, seperti etilen glikol (bahan antibeku), vinil klorida (bahan pembuatan PVC), dan stirena (bahan pembuatan polistirena).
-
Industri Makanan: Hidrogenasi digunakan untuk mengubah minyak nabati cair menjadi lemak padat (margarin). Reaksi adisi juga digunakan untuk menghasilkan berbagai macam bahan tambahan makanan.
-
Industri Farmasi: Reaksi adisi digunakan dalam sintesis berbagai macam obat-obatan.
-
Industri Polimer: Polimerisasi adisi digunakan untuk menghasilkan berbagai macam plastik, karet, dan resin.
-
Sintesis Organik: Reaksi adisi merupakan salah satu reaksi yang paling penting dalam sintesis organik, memungkinkan pembentukan ikatan karbon-karbon dan pengenalan gugus fungsi ke dalam molekul organik.
Kesimpulan
Reaksi adisi adalah reaksi fundamental dalam kimia dengan aplikasi yang sangat luas. Dari pembuatan margarin hingga produksi plastik, reaksi ini memainkan peran penting dalam kehidupan sehari-hari kita. Memahami mekanisme dan contoh-contoh reaksi adisi memberikan kita wawasan yang lebih dalam tentang dunia kimia dan bagaimana berbagai produk yang kita gunakan diproduksi. Jadi, lain kali kamu lihat botol plastik atau makan roti dengan margarin, ingatlah bahwa semua itu berkat reaksi adisi!
Apakah kamu punya pengalaman menarik atau pertanyaan seputar reaksi adisi? Yuk, bagikan di kolom komentar!
FAQ (Frequently Asked Questions)
1. Apa perbedaan antara reaksi adisi dan reaksi substitusi?
Reaksi adisi adalah reaksi penggabungan, di mana dua atau lebih molekul bergabung menjadi satu molekul yang lebih besar. Sementara itu, reaksi substitusi adalah reaksi penggantian, di mana satu atom atau gugus atom digantikan oleh atom atau gugus atom lain. Reaksi adisi biasanya terjadi pada senyawa dengan ikatan rangkap, sedangkan reaksi substitusi biasanya terjadi pada senyawa dengan ikatan tunggal.
2. Apa itu aturan Markovnikov?
Aturan Markovnikov menyatakan bahwa dalam reaksi adisi hidrogen halida (seperti HCl atau HBr) pada alkena, atom hidrogen akan terikat pada atom karbon yang memiliki jumlah atom hidrogen lebih banyak. Dengan kata lain, atom hidrogen akan "memilih" atom karbon yang sudah lebih kaya hidrogen.
3. Mengapa katalis diperlukan dalam beberapa reaksi adisi?
Katalis diperlukan untuk mempercepat laju reaksi. Dalam beberapa reaksi adisi, energi aktivasi (energi yang diperlukan untuk memulai reaksi) sangat tinggi. Katalis menurunkan energi aktivasi, sehingga reaksi dapat berlangsung lebih cepat pada suhu yang lebih rendah. Katalis tidak dikonsumsi dalam reaksi, sehingga dapat digunakan berulang kali.